新产品丨新型胱胺核聚酰胺胺(PAMAM)
在精准医疗与智能递药快速发展的当下,载体材料的创新与功能响应性至关重要。胱胺核聚酰胺-胺树状大分子(胱胺核PAMAM)以二硫键为核心、树枝状分支结构为特色,在生物医药领域极具潜力。其独特设计赋予材料肿瘤微环境响应性与可降解性,规避生物蓄积风险。凭借“结构、功能、代谢”三方面优势,胱胺核PAMAM在药物靶向递送、基因治疗等领域发挥关键作用,为肿瘤治疗、基因递送难题提供新方案。
2.基因递送的分子机制
胱胺核PAMAM的树形分支结构可通过静电相互作用与带负电的核酸形成纳米复合物,其结合能力取决于表面氨基的质子化程度——在生理pH条件下,部分氨基质子化(-NH3⁺)形成的正电荷与核酸磷酸基团(-PO4⁻)的静电引力,可有效压缩核酸分子尺寸,避免核酸酶降解。核定位信号(NLS)肽段的修饰可引导复合物通过核孔复合体进入细胞核,提升转染效率,而二硫键的还原响应性则确保复合物在胞质内解体释放核酸,减少对正常细胞功能的干扰。
低细胞毒性源于胱胺核的可降解特性:二硫键在细胞内还原条件下的断裂产物为小分子胱胺衍生物,可通过代谢途径排出,避免传统非降解载体的累积毒性。通过调控分子代数与表面基团比例(如引入羟基、聚乙二醇链),可进一步降低表面正电荷密度,减少对细胞膜的破坏,实现毒性与转染效率的平衡。
在生物医药领域,载体材料的结构特性与功能表现是技术落地的关键。胱胺核聚酰胺-胺树状大分子(胱胺核PAMAM)因核心二硫键结构和树枝状分支形态,在生物医药场景中具备应用基础。其在肿瘤微环境响应、生物降解性等方面的特点,使其在药物靶向递送、基因治疗等领域有实际应用可能。晨源分子研发的胱胺核PAMAM产品,相关参数可支撑上述应用场景的技术实现。
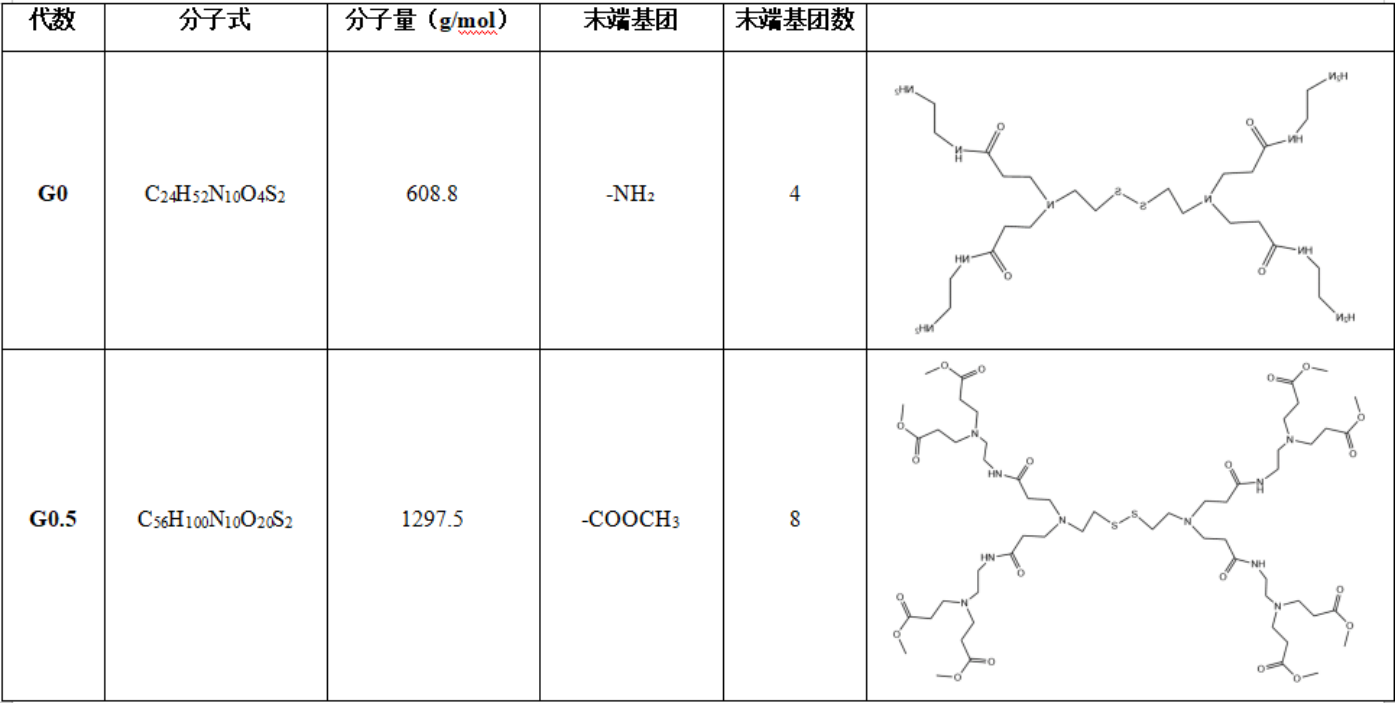
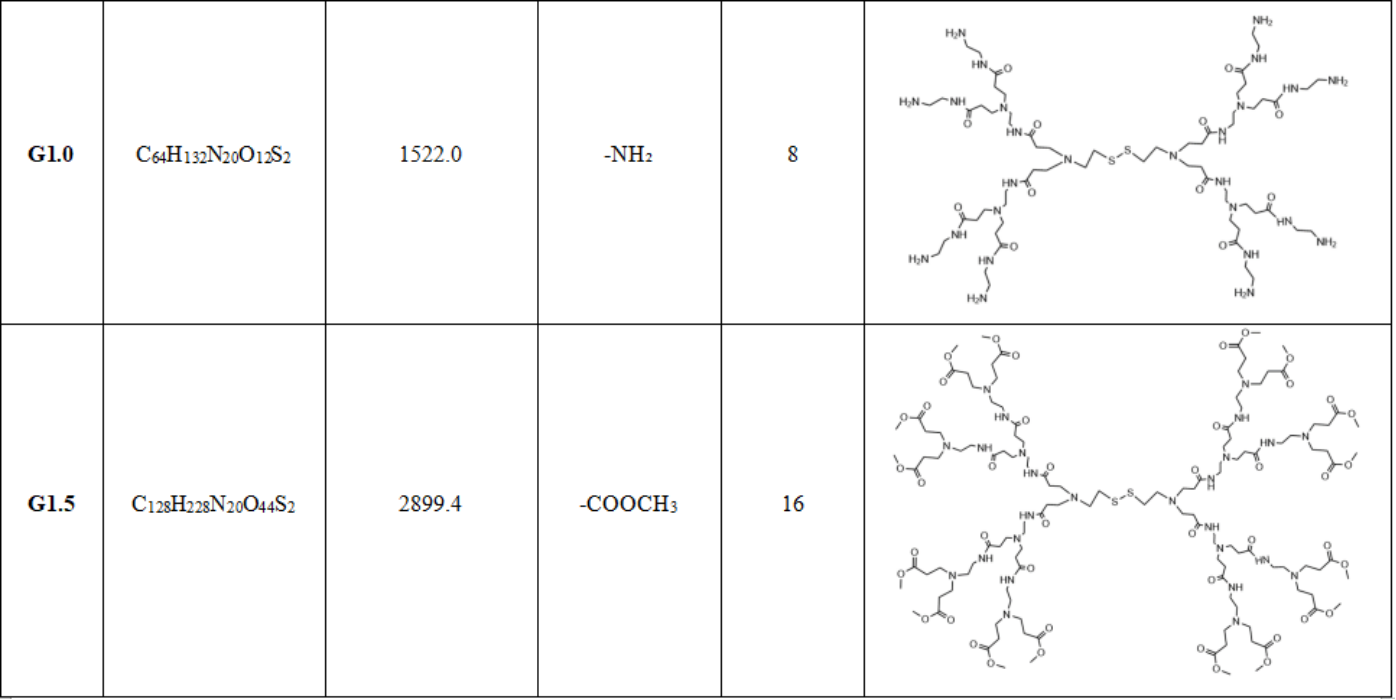
胱胺核的PAMAM产品
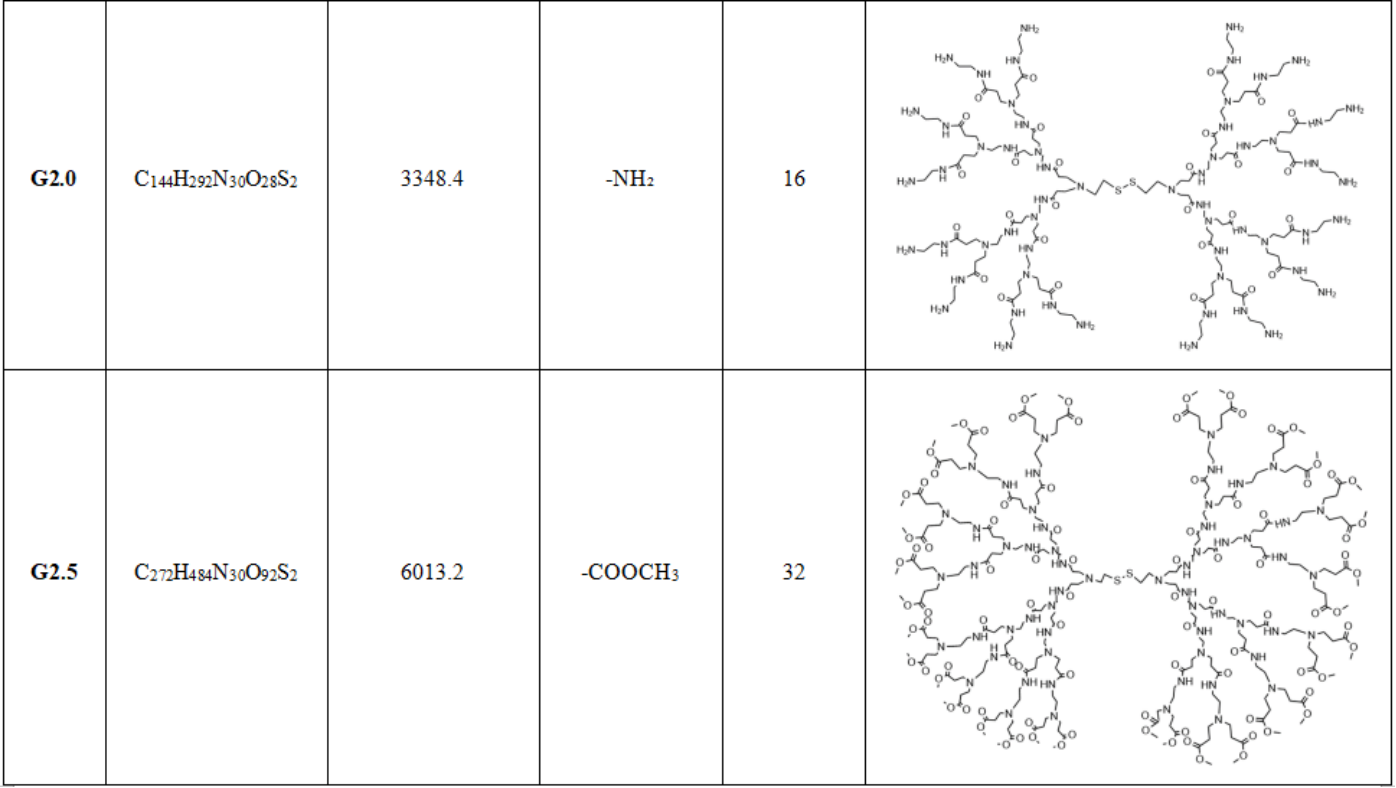
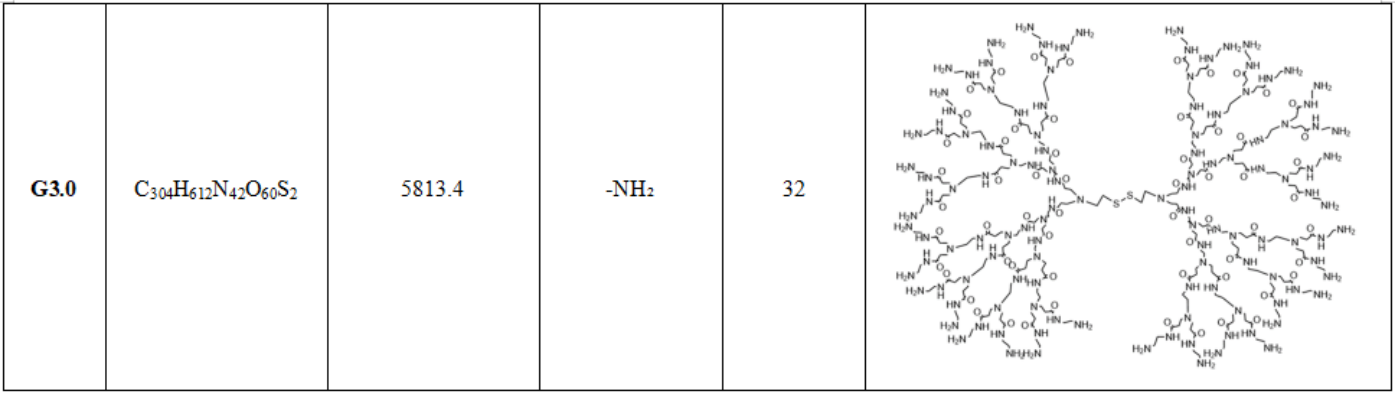
联系我们
电话:0631-5582236
地址:山东威海临港经济技术开发区草庙子369-13号
本站部分内容来源于网络,如果您认为我们侵犯了您的版权请告知,我们将立即删除